- A+
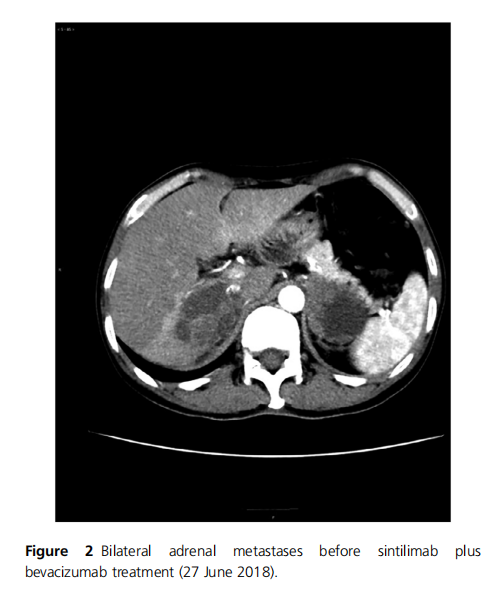
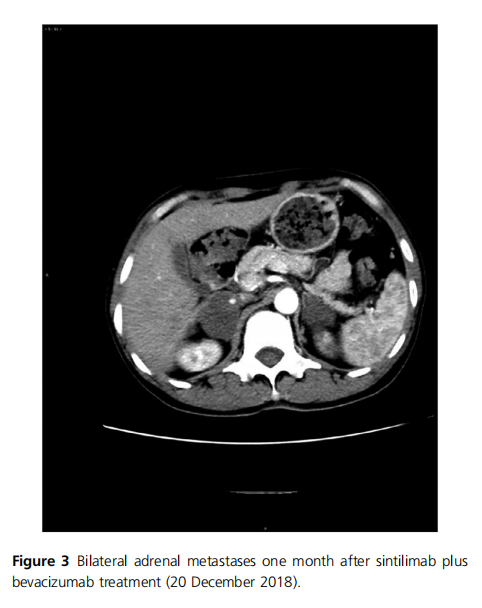
在免疫与靶向无缘的定论下,该案例还是给了我们不一样的治疗视角。靶向耐药是目前我们基因突变肺癌人群必须面对的结局。如何更好地在靶向后运用好低毒的免疫药物,是我们一大挑战命题。如果单免不行,患者朋友又不愿添加化疗,我们该如何提升免疫疗效呢?该案例提出的免疫+抗血管的模式就给了我们很好的治疗思路。这种模式在目前肺癌之外的很多癌种都得到了认可。比如2019年4月19日,美国食品药品监督管理局批准PD-1抗体Keytruda联合阿昔替尼一线用于晚期肾细胞癌患者,成为首个获得监管部门认可的PD-1+血管生成抑制剂的联合疗法。今年的阿替利珠单抗联合贝伐单抗获批了肝癌一线治疗。以及仑伐替尼+帕博利珠单抗在肝癌、子宫内膜癌;纳武利尤单抗联合瑞戈非尼在MSS结直肠癌,都获得不错的成绩。国内的小分子抗血管原研药物阿帕替尼/安罗替尼联合PD1单抗更是在肺癌、肝癌、肉瘤等领域得出过数据。下面列举两个肺癌方面的免疫+抗血管联合的研究:
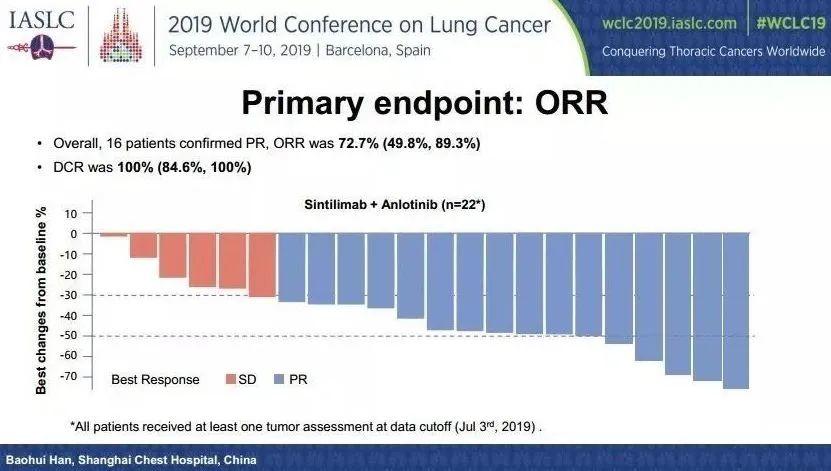
1. 信迪利单抗联合安罗替尼一线治疗无基因突变的晚期NSCLC,有效率72.7%。
2019年WCLC(世界肺癌大会)上,上海市胸科医院韩宝惠教授口头汇报了信迪利单抗联合安罗替尼一线治疗驱动基因(EGFR/ALK/ROS1)阴性晚期非小细胞肺癌(NSCLC) 的Ⅰ期临床研究结果,主要研究终点ORR高达72.7%,DCR达100%。
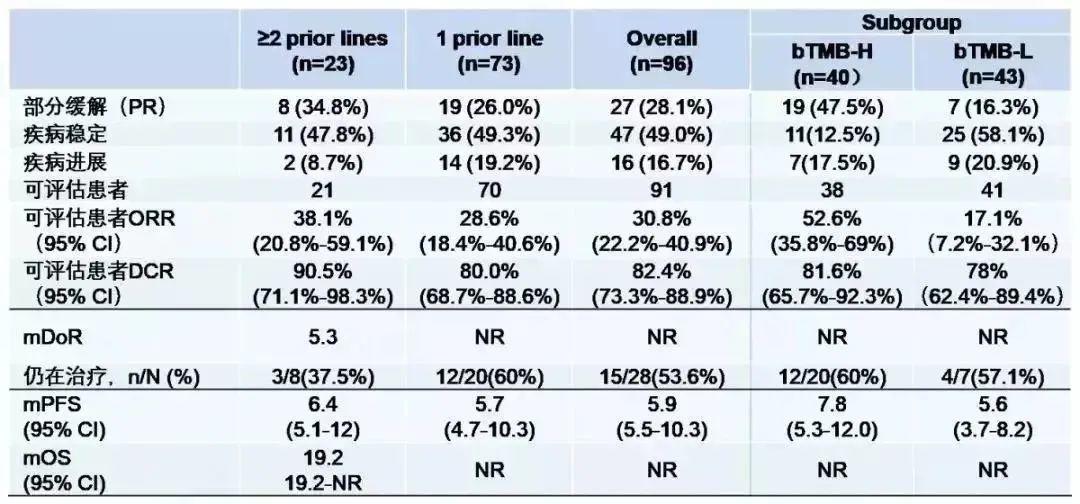
2. 卡瑞利珠单抗联合阿帕替尼后线治疗非鳞NSCLC,有效率为30.8%
该试验纳入96例晚期非鳞NSCLC患者,其中23例接受过二线及以上的系统治疗,73例接受过一线治疗。结果显示,在91例可评估的患者中,总ORR为30.8%,中位PFS为5.9个月。在所有96例患者中,83例患者进行了bTMB检测,通过ROC曲线计算其临界值为1.54 muts/Mb。可评估的高bTMB患者ORR达52.6%。在数据收集截止时,有29例受试者仍在接受治疗。
事无绝对,综合评估患者当下分子指标,科学选药
该EGFR的免疫使用案例,与近期我们报道的一例ALK阳性患者使用PD1药物获得CR,有相似之处。虽然患者为公认的EGFR/ALK阳性患者,靶向耐药后,但是患者同时具有PDL1的阳性表达,因此也可选用免疫药物进行尝试。提示我们在诊疗患者中,应充分检测我们目前所知的有用指标,综合判断,综合选药,不要一味定性。
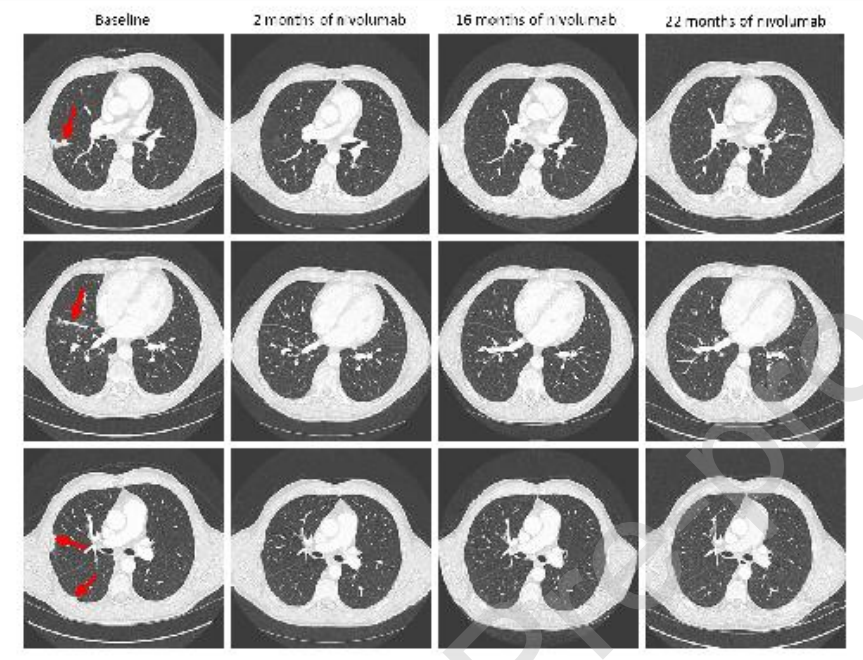
ALK阳性患者,靶向、化疗均耐药后,PDL1表达100%,采用O药治疗, 2个月达到完全缓解(CR),持续近2年(图2和3)。患者出现左颈淋巴结转移后,采用立体定向放射疗法(SBRT)治疗(36 Gy),并继续使用纳武单抗。
医无定论,不断探索,治愈前行!
EGFR靶向耐药研究推荐:
信迪利单抗联合抗血管药IBI305+培美曲赛+铂类治疗EGFR-TKI治疗失败的EGFR突变的局晚期或转移性非鳞非小细胞肺癌患者。感兴趣的患者朋友可以点击下文的阅读原文报名参加。
本篇文章来源于微信公众号: 找药宝典