- A+
在人类历史上,手术作为一种治疗手段,已经存在了3000多年,放疗使用了120余年,化疗也有70余年的历史。这三种治疗方法被誉为癌症治疗的“三驾马车”,不过这三种疗法仅救治了不到一半的癌症患者。
在上个世纪,随着分子生物学的发展,科学家和医生对癌症有了长足的认识,免疫系统成为科学家和医生学习的对象,能靶向癌细胞的单克隆抗体药物应运而生。
1997年,首个治疗癌症的单抗获批上市,开启了癌症治疗的全新方式。
抗体偶联药物的诞生
伴随着单抗类药物诞生的,还有另一种激动人心的抗癌药物——抗体偶联药物。
实际上,早在100多年前,诺奖得主保罗·埃尔利希(Paul Ehrlich)就提出了“魔法子弹”的概念[1]。他认为,如果将能杀死癌细胞的药物安装在特异性靶向癌细胞的载体上,就有望专一地杀死癌细胞,而不伤害人体正常细胞。

▲ Paul Ehrlich(来源:wiki)
这个治疗癌症的概念非常诱人,不过在很长的一段时间里,它也只是停留在概念阶段。直到具有靶向性的单克隆抗体出现之后,很多科学家开始考虑将化疗药物挂在单抗上制作狙杀癌细胞的“魔法子弹”。
从文献资料来看,关于抗体偶联药物的最早报道出现在1958年[1],在1980年代,甚至有科学家用基于小鼠免疫球蛋白G的抗体偶联药物开展了临床研究[2]。不过,早期的抗体偶联药物基本都以失败告终。
进入二十一世纪之后,抗体偶联药物终于迎来了属于自己的时代。
2000年,Gemtuzumab ozogamicin(Mylotarg)成为第一个获得FDA批准的抗体偶联药物,也是我们常说的第一代抗体偶联药物。不过,由于Mylotarg副作用大且疗效不显著,2010年撤市(2017年重新获FDA批准上市)。
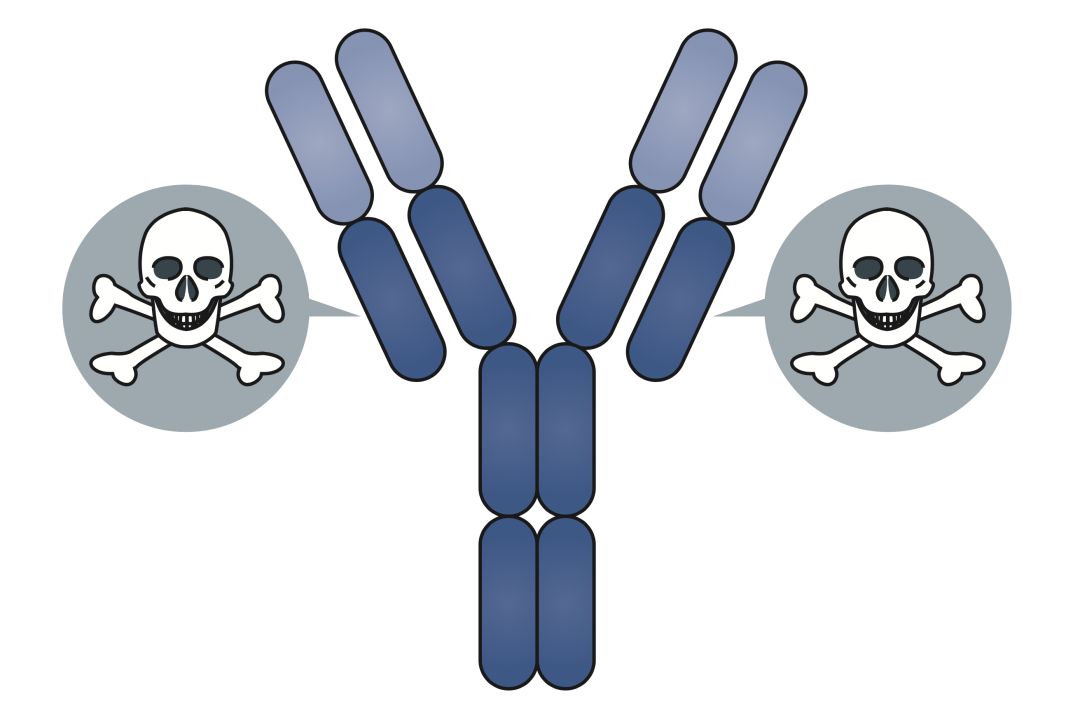
▲ 抗体偶联药物示意图(图源:10.1038/nrd.2017.227)
在Mylotarg撤市后的一年,也就是2011年,第二代抗体偶联药物Brentuximab vedotin(Adcetris)获得FDA的批准,用于治疗霍奇金淋巴瘤和复发性间变性大细胞淋巴瘤。直到今天,Adcetris还是一种重要的抗癌药物。从某种意义上讲,Adcetris才是真正的首个获批上市的抗体偶联药物。
接下来的内容,我们就以Adcetris为例,给大家系统地介绍下抗体偶联药物。
Adcetris的真面目
从埃尔利希对“魔法子弹”的描述中,我们不难看出,抗体偶联药物这颗“魔法子弹”由三部分组成:单抗,化疗药物,以及将前面二位连接起来的元件(它有个好听的名字叫连接子)。
咱们先来看看Adcetris的结构。
它是由靶向CD30的单抗cAC10(SGN-30)与阻止微管蛋白聚合进而抑制有丝分裂的Monomethyl auristatin E(MMAE),通过一个可被蛋白酶切割的接头连接而成。形状如下图所示。
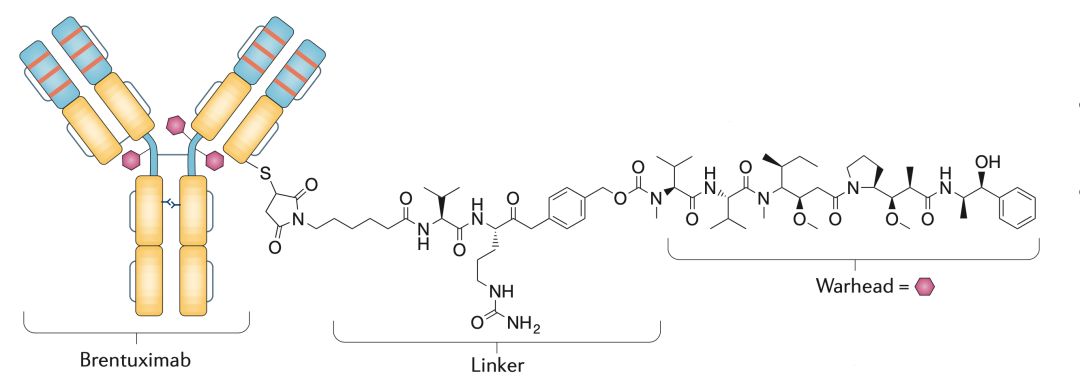
▲ BV的结构插图(图源:10.1038/nrd.2016.268)
CD30是肿瘤坏死因子受体(TNFR)超家族的一种跨膜蛋白,科学家已经在好几种恶性肿瘤中检测到它的存在,例如霍奇金淋巴瘤,间变性大细胞淋巴瘤(ALCL),B细胞来源的非霍奇金淋巴瘤的某些亚型,以及成熟的T细胞淋巴瘤等[3]。
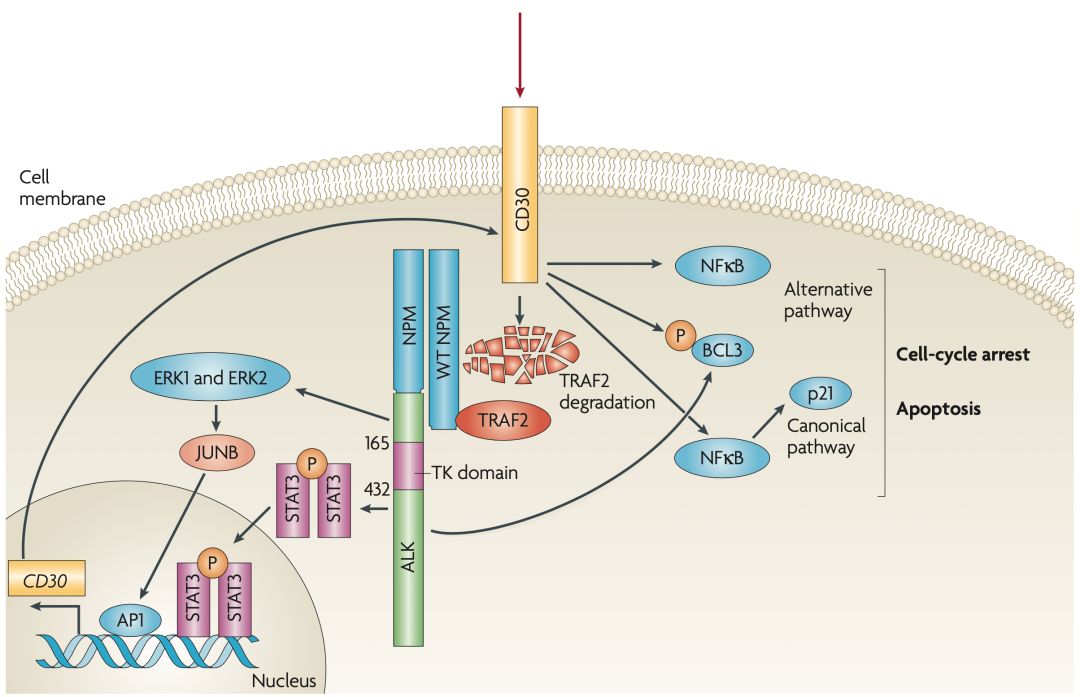
▲ CD30信号通路(图源:10.1038/nrc2291 )
CD30在淋巴细胞亚群中受限制的表达,让它成为治疗淋巴系统肿瘤的理想靶点。这就意味着Adcetris靶向癌细胞的特异性有了保证。
而MMAE,则是奥瑞他汀类的微管蛋白活性抑制剂。它能使癌细胞在分裂时,两个子细胞不能正常分配遗传物质,从而导致癌细胞分裂半途而废,最终癌细胞因遗传物质混乱而死[4]。
那么MMAE是如何挂在CD30单抗cAC10上形成Adcetris的呢?
在揭开谜底之前,我们需要知道两个问题。第一,连接抗体与药物的元件不能影响到药物本身的作用;第二,为了尽可能的减小药物的副作用,连接子不能在药物还在血液里时就断了。
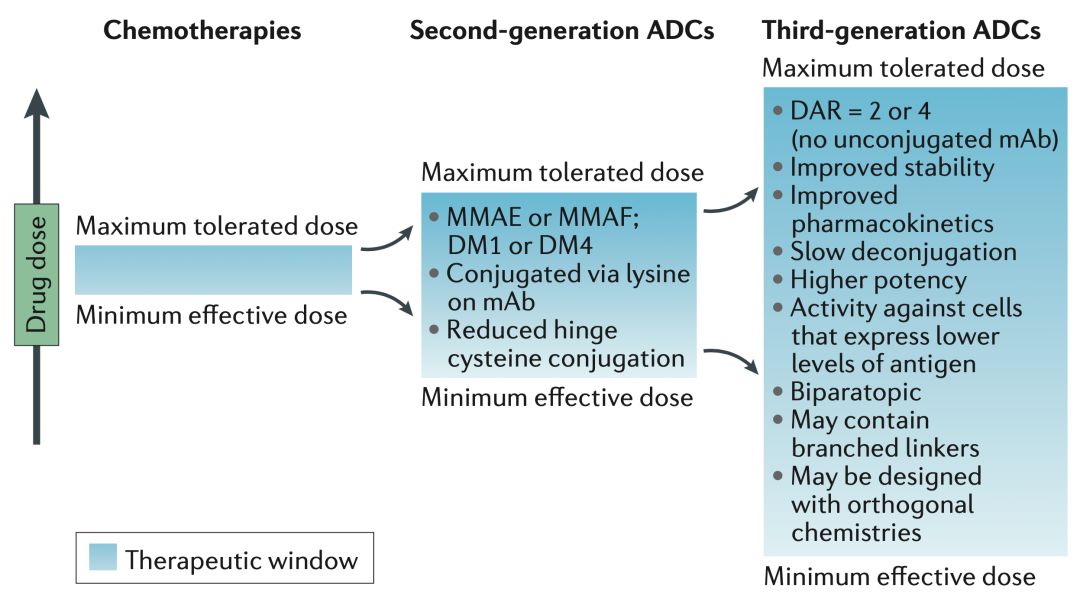
▲ ADC治疗窗口期更大(图源:10.1038/nrd.2016.268)
对于Adcetris而言,满足上述两个条件的是由瓜氨酸-缬氨酸组成的二肽连接子。
首先,这个二肽的连接子足够小,基本不会影响到单抗和MMAE;其次,这个二肽在血浆中高度稳定,在被CD30阳性细胞内化后可被溶酶体酶快速有效地切割,发挥杀灭癌细胞的作用[5]。
Adcetris的“必杀技”
有了以上背景知识,接下来我们可以看看Adcetris对癌细胞的5个“必杀技”。
第一招:MMAE毒杀癌细胞。
关于这一招,简单的描述是这样的:医生将Adcetris注射到患者体内之后,在CD30抗体的导航下,Adcetris迅速锁定携带CD30的癌细胞,并于CD30结合;紧接着,癌细胞会把Adcetris吞进细胞内部,Adcetris遇到细胞内部的溶酶体酶之后,二肽连接子就会被切断,MMAE立即抑制微管蛋白活性,让癌细胞的分裂半途而废,最终混乱而死[6]。
第二招:MMAE旁杀肿瘤组织细胞。
奇点的读者一定都知道,肿瘤里面不仅有癌细胞,还有很多肿瘤基质细胞,它们支撑着肿瘤的生长的发展,对肿瘤非常重要,消灭它们能在一定程度上起到打击肿瘤的作用。
在第一招里面,MMAE杀死癌细胞之后,随着癌细胞破裂,释放到肿瘤微环境中。这个MMAE还有个特点,它可以自由穿过细胞膜。这就意味着,被癌细胞释放的一部分MMAE,会自由渗透到肿瘤的其他细胞中,包括CD30阴性的癌细胞,肿瘤相关的其他各种基质细胞,都有可能被MMAE毒杀[6]。
这一招很厉害,因为即使肿瘤中很多癌细胞没有CD30,它们也难逃被MMAE击杀的命运。
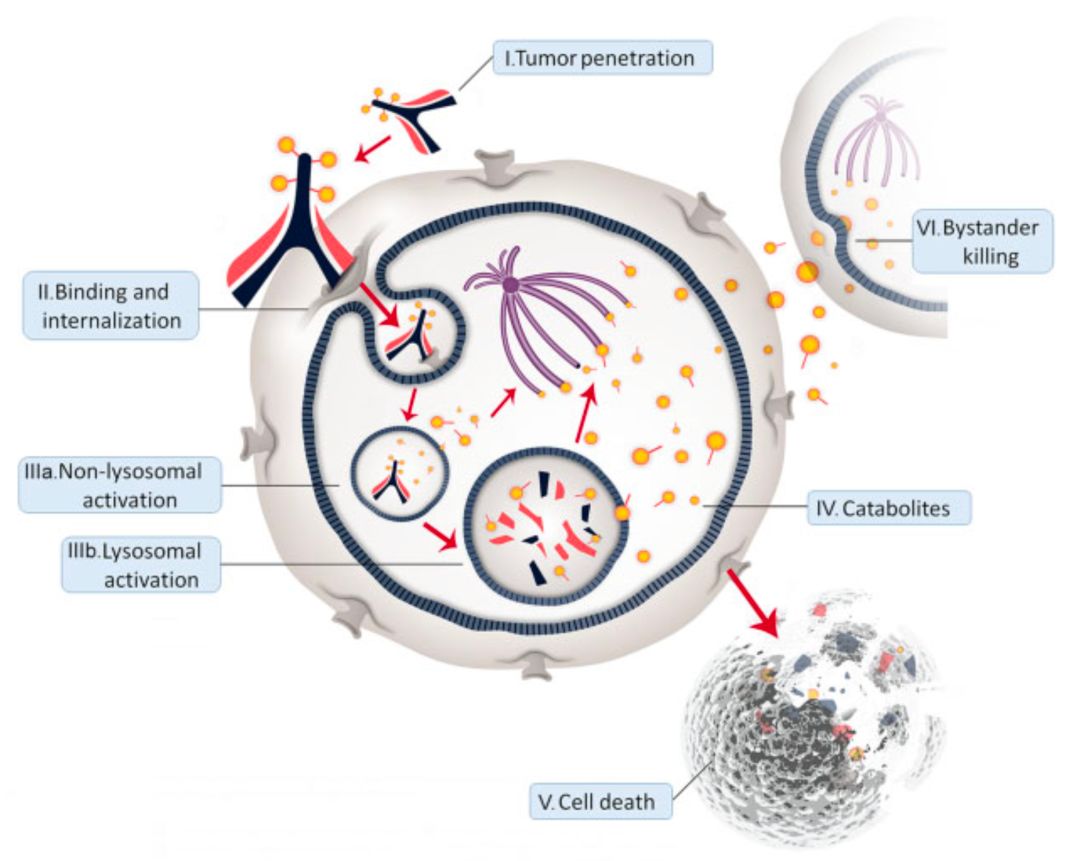
▲ 抗体偶联药物杀癌细胞机制图(图源:10.1093/jnci/djz035)
第三招和第四招:CD30单抗cAC10两招诛杀癌细胞[3]。
Adcetris中的CD30抗体并不简单,它不仅是MMAE的定向运载工具,还是癌细胞的催命符。对于CD30单抗cAC10而言,它作为一个单抗,本身还具有抗体依赖性细胞吞噬作用(ADCP)。啥意思呢,就是cAC10结合在癌细胞表面之后,会召集巨噬细胞等吃掉癌细胞。
除此之外,CD30单抗cAC10还有个技能——阻断CD30相关的信号通路,这一招也能抑制肿瘤的生长。
第五招:调节免疫系统抗癌。
一般情况下,正常的细胞死亡都是非免疫原性的,不会促发大规模的免疫反应。但是科学家发现,Adcetris可以诱导免疫原性细胞死亡,释放一些免疫相关信号分子,重启肿瘤微环境中被抑制的免疫反应[7]。
研究人员甚至已经发现,Adcetris治疗可以增加细胞毒性T细胞和NK细胞的数量,与PD-1抗体联合使用,抗癌效果更强大[8]。
以上就是Adcetris的组成和抗癌机制,虽然看上去很简单,但是抗体偶联药物的研发并没有那么容易。
抗体偶联药物之难
首先得在癌细胞表面寻找一个合适的靶点,以及针对这个靶点的抗体,化疗药物连接到抗体上之后,还不能影响抗体的作用。
其次必须得有一个合适的连接子。这个连接子在血液中必须稳定,以降低药物的毒副作用。
最后还得控制好药物与抗体的偶联比例。从理论上说,每个抗体上大约有80-100个可偶联的氨基酸残基。前期的研究表明,抗体上挂太多药物不行;挂太少,甚至很多抗体不挂药物,也不行。这两种情况都会影响药物的安全性。
从包括Adcetris在内的成功抗体偶联药物来看,药物与抗体的偶联比例最好控制在3.5-4之间。对于Adcetris而言,平均每个抗体上带有4个MMAE基团[5]。
总之,抗体偶联药物是抗癌药物发展最迅速的领域之一,研究人员也对它寄予厚望。期待这颗“魔法子弹”最终能给癌症致命的一击。
参考资料:
[1].Panowski S, Bhakta S, Raab H, et al. Site-specific antibody drug conjugates for cancer therapy[J]. mAbs, 2014, 6(1): 34-45.
[2].Perez H L, Cardarelli P M, Deshpande S, et al. Antibody-drug conjugates: current status and future directions.[J]. Drug Discovery Today, 2014, 19(7): 869-881.
[3].van de Donk N W C J, Dhimolea E. Brentuximab vedotin[C]//MAbs. Taylor & Francis, 2012, 4(4): 458-465.
[4].Francisco J A, Cerveny C G, Meyer D L, et al. cAC10-vcMMAE, an anti-CD30–monomethyl auristatin E conjugate with potent and selective antitumor activity[J]. Blood, 2003, 102(4): 1458-1465.
[5].Doronina S O, Toki B E, Torgov M, et al. Development of potent monoclonal antibody auristatin conjugates for cancer therapy[J]. Nature Biotechnology, 2003, 21(7): 778-784.
[6].Okeley N M, Miyamoto J B, Zhang X, et al. Intracellular Activation of SGN-35, a Potent Anti-CD30 Antibody-Drug Conjugate[J]. Clinical Cancer Research, 2010, 16(3): 888-897.
[7].Shyra J. Gardai, Angela Epp, Che-Leung Law. Brentuximab vedotin-mediated immunogenic cell death. [abstract]. In: Proceedings of the 106th Annual Meeting of the American Association for Cancer Research; 2015 Apr 18-22; Philadelphia, PA. Philadelphia (PA): AACR; Cancer Res 2015;75(15 Suppl):Abstract nr 2469. doi:10.1158/1538-7445.AM2015-2469
[8].Anthony T. Cao, Che-Leung Law, Shyra J. Gardai, Ryan A. Heiser. Brentuximab vedotin-driven immunogenic cell death enhances antitumor immune responses, and is potentiated by PD1 inhibition in vivo [abstract]. In: Proceedings of the American Association for Cancer Research Annual Meeting 2017; 2017 Apr 1-5; Washington, DC. Philadelphia (PA): AACR; Cancer Res 2017;77(13 Suppl):Abstract nr 5588. doi:10.1158/1538-7445.AM2017-5588