- A+

让我们成为您抗肿瘤路上的医学地图
从此不再走弯路

我们当然知道大多数患者在迫切想知道答案的同时,却没有额外的精力去学习肿瘤诊治的知识。但是,用“好”和“坏”这种非黑即白的方式理解世界总会遇到瓶颈。
所以,在真正回答问题之前用基本事实构建一个简单的逻辑:
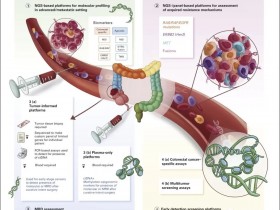
基因突变是肿瘤形成的基础,有些已经被发现,还有更多未被发现;有些对肿瘤的发生发展至关重要(驱动基因),有些则不然。
医学的发展已经了解了其中一部分机制(免疫检查点),但仍有许多未知。
这些药物本质上是针对肿瘤的某个特征研发出相应的药物,这也就意味着它们只能不同程度的覆盖一部分患者,而呈现出一种药物筛选患者的模式。
对于早期肿瘤,肿瘤局限在局部,医生可通过手术切除方式,相对彻底的解决肿瘤(精准打击)。
但肿瘤与其他疾病不同的是,肿瘤细胞的散播可以在其他部位产生新的肿瘤,而形成转移性肿瘤。这种晚期肿瘤通常被认为手术的价值不大,所以需要进行药物系统治疗(广泛打击)。
而靶向药理论上只针对只有肿瘤才会出现基因突变及相应的生物学效应起作用;免疫治疗药物则是破除肿瘤的伪装,调动身体最“智能”的免疫系统攻击肿瘤从而起到抗肿瘤的作用。
这种在微观上药物对肿瘤不同程度的选择性,以及宏观上根据患者不同特征使用不同药物这两个层面的事实构建了“精准医疗”这个词的内核。
但目前中国患者能使用的驱动基因靶向药也只有EGFR、ALK、ROS1三类(海外还有BRAF V600E、KRAS两类)。
国内患者可使用的EGFR抑制剂有5种、ALK抑制剂2种、ROS1抑制剂1种。
当一位患者在表达“肺Ca没有基因突变”的时候,其实真正的含义是:处于肺Ca晚期,需要系统治疗,但经基因检测没有发现EGFR、ALK、ROS1基因突变。
这些基因突变本质上是肿瘤具有的某种特征,但不是所有肿瘤的普遍属性。所以,有这些基因突变的患者是少数,而没有这些基因突变患者才是大多数。
有没有这些基因突变最大的区别就是能不能使用靶向药。
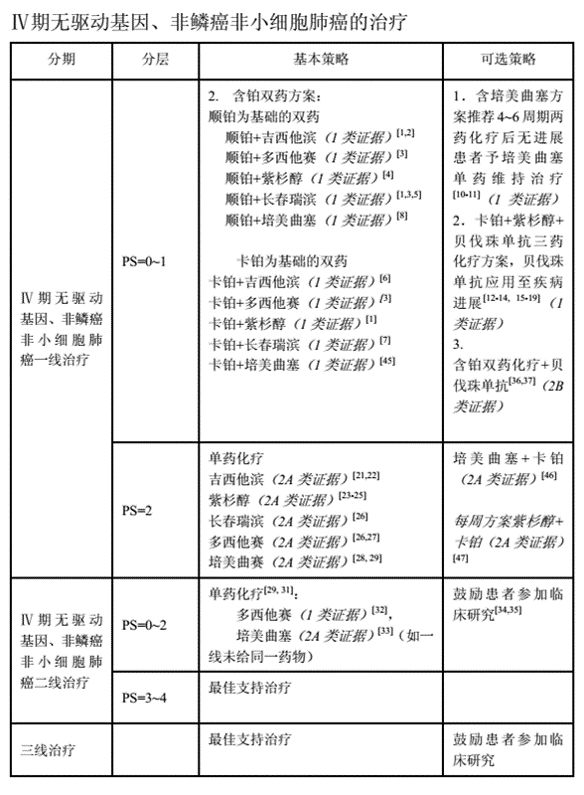
不过,使用靶向药物总是会要求患者具有相应的基因突变,也就是所谓的药物筛选患者。可靶向药就在那里,为什么不让无驱动基因突变的患者试试呢?
现有证据表明,无驱动基因突变的患者使用EGFR抑制剂、ALK抑制剂的效果与标准的含铂双药化疗相比并没有优势,所以患者经基因检测确认驱动基因阴性后,医生一般不会再考虑靶向药,而选择化疗作为患者接受的一线治疗。
“所以,不能吃靶向药就是不好呗?”
也未必
疗效
不能接受靶向药治疗、只能化疗不代表疗效一定差。
在EGFR基因突变的患者中,使用第一、二代EGFR抑制剂患者的中位无进展生存期普遍在10个月左右,化疗患者的中位无进展生存期则在6~7个月左右。这样的对比自然说明EGFR基因突变的患者应该选用EGFR抑制剂。
但在无驱动基因突变的患者中,采用培美曲赛联合顺铂的化疗方案也达到了10~12个月的中位无进展生存期(鳞肿瘤除外)。
的确,试验的患者不同没办法直接比较。但对接受治疗的患者而言,无论是否有驱动基因突变,都可以有10个月的无进展生存期。
从这个角度上,无驱动基因突变不算“坏”。
后续治疗选择
靶向药耐药是最让医生和患者头痛的问题,特别是EGFR抑制剂,在经过8~13 个月的疾病控制后几乎所有的患者都会耐药。
目前,在中国EGFR突变的患者一线治疗进展后,会根据进展的模式继续EGFR抑制剂治疗或者升级为第三代EGFR抑制剂奥希替尼。说起来轻松,但实际上这款药物月治疗费用在5万以上,不是一般家庭能承受的。如果不能选择奥希替尼,又没有其他有效的靶向药,结果就是放弃针对EGFR基因突变的治疗。
在无驱动基因突变的患者中,患者接受含铂双药化疗失败后,可选的有单药化疗以及最新批准的免疫治疗药物纳武利尤单抗。特别提醒,纳武利尤单抗的月治疗费用在9万左右。
高价药的存在只是对患者经济实力的考验,但不是必须要越过的障碍。从全局来看,有驱动基因突变的患者比无驱动基因突变的患者多了一些用药的选择,理论上肿瘤得到控制的时间更长。
从这个角度上,无驱动基因突变是“坏”。
医药支出
这的确是最值得对比的方面,但遗憾的是,由于治疗方案和用药选择的不同,基于假设的计算是没有太多意义的。
但要说的是,在第一代靶向药问世多年的今天,仿制药和医保两方面的因素已经让驱动基因突变的肺Ca患者不再需要支出高额的药费。有报道指出,进入医保后一些靶向药的日治疗费用可降至60元/天,这样的价格可以说是相当亲民了。
而化疗的费用则根据用药方案差异较大。疗效好的化疗药物,特别是进口原研药甚至比进口原研靶向药物还要贵。所以,化疗和靶向治疗哪种治疗方法更经济是不能一概而论的。可以说在晚期肺Ca的治疗中,接受化疗并不意味着绝对的价格优势。
从这个角度上,无驱动基因突变不算“好”
“这样看来,没基因突变还是不是什么好事啊。”
事实可能确实如此。我们的确想给那些没有驱动基因突变的肺Ca患者一些信心,但具有EGFR、ALK这种基因突变的患者确实比没有基因突变的患者“幸运”。
其实,没有驱动基因突变的患者也不用觉得有什么损失,因为没有基因突变本身也是一种特征。目前免疫治疗药物作为抗肿瘤药物研发的热点,往往在临床试验中招募的都是无驱动基因突变的患者,医学指南也会建议无基因突变的患者在缺乏有效治疗方案的情况下更早参加临床试验。
所以,没有驱动基因突变的患者也有属于自己的未来和治疗机会。

中国临床肿瘤学会(CSCO) 原发性肺Ca诊疗指南2017.V1
NCCN临床实践指南:非小细胞肺Ca(2018.V4)